Достижения науки стремительно изменяют схемы лечения пациентов с онкопатологией. Рассмотрим, что такое комплексное геномное профилирование, и почему важно проводить исследование опухолей на генетические мутации.
Содержание статьи
Биологическое разнообразие опухолей – проблема или решение? Почему важно проводить геномное профилирование опухолей Комплексное геномное профилирование — подход, объединяющий новейшие методы диагностики и лечения рака Заключение
Современная медицина с каждым годом узнает все больше о генетических предпосылках онкологических заболеваний. Наука движется в сторону выявления и тщательного изучения мутаций, лежащих в основе рака. Теоретические наработки активно внедряют в практическую медицину, которая становится все более персонализированной. Новые методы позволяют подобрать для каждого пациента с онкопатологией максимально эффективное индивидуальное лечение с учетом особенностей течения именно его заболевания. Важную роль в этом играет комплексное геномное профилирование (КГП). Этот подход позволяет составить полную картину генетических изменений внутри каждой опухоли и на основе биоинформационного анализа и экспертного мнения получить практические рекомендации по эффективному и безопасному лечению.
В этой статье мы разберем основные понятия, связанные с генетикой рака, поговорим о видах мутаций при опухолях и расскажем, как КГП помогает их обнаружить.
Биологическое разнообразие опухолей – проблема или решение?
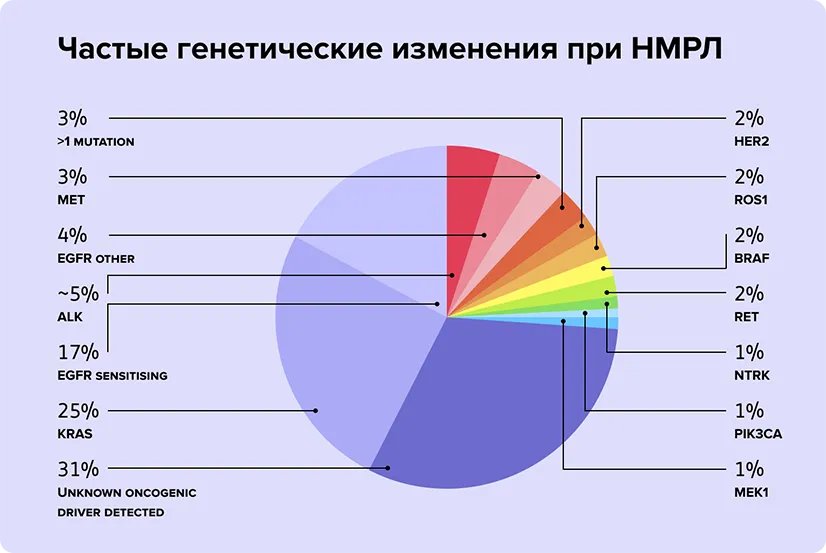
Под общим термином «рак» в действительности понимают огромное количество заболеваний. Более того, злокачественный процесс в одном органе может иметь множество подтипов. Например, один только подтип рака легкого, который называют немелкоклеточным, может запускать мутации как минимум в 13 изученных генах — они составляют основные 2/3 «виновников» этой болезни. А сколько генов, вовлеченных в развитие этой болезни, еще не изучено1?!
То есть существует множество молекулярных путей, сбой в которых приводит к тому, что нормальные клетки становятся злокачественными. Кроме того, в одной опухоли могут сочетаться разные мутации. С одной стороны, биологическое разнообразие опухолей — проблема, потому что нужно понять, какой вид заболевания у конкретного больного и из множества вариантов лечения выбрать оптимальный. С другой стороны, современные методы терапии позволяют прицельно воздействовать на конкретные молекулярные «поломки». И если точно подобрать «ключ», результат лечения будет очень хорошим.
Почему важно проводить геномное профилирование опухолей
Почему важно знать генетический профиль опухоли и связанные с ней мутации? Дело в том, что лечение рака очень усложнилось. В 2017 году в разработке находилось более 700 лекарственных молекул, действие которых направлено на разные пути образования опухолей2. Для подбора эффективного лекарства необходимо знать, какие именно генетические мутации есть в конкретном случае заболевания. Для этого проводят секвенирование — определение последовательностей «кирпичиков» (нуклеотидов), из которых состоит ДНК (генетический код) опухолевой клетки.
Секвенирование нового поколения расширяет возможности геномного профилирования опухолей
Передовой метод секвенирования нового поколения (с англ. NGS — next generation sequencing) дает возможность исследованием одного биоматериала провести комплексное геномное профилирование опухоли, т.е. обнаружить все возможные генетические изменения в большом количестве онкозначимых генов. При NGS происходит параллельное считывание миллионов мелких участков ДНК, их сравнение с эталонным геномом с помощью биоинформатического анализа.
Если с помощью прежних методов, таких как полимеразная цепная реакция (ПЦР), иммуногистохимическое исследование (ИГХ) или флуоресцентная гибридизация in situ (FISH) можно было исследовать изменения в одном или нескольких генах, то NGS позволяет исследовать практически весь геном за один раз3, 4.
Комплексное геномное профилирование — подход, объединяющий новейшие методы диагностики и лечения рака
С помощью КГП можно проанализировать все классы генетических изменений во всех известных онкозначимых генах. Таким образом, значительно повышается точность выявления мутаций в генах и определения типа опухоли. Так, КГП позволяет выявить до 37% больше пациентов с изменениями в генах при меланоме и до 35% больше при некоторых видах рака легкого по сравнению с методами ПЦР, ИГХ, FISH и другими традиционными методами5–7. Существуют тесты, позволяющие определить изменения (мутации) в 324 генах, связанных с раком.
КГП обеспечивает сопроводительную диагностику — дает информацию для безопасного и эффективного использования соответствующего лечения.
То есть, проведя один тест, можно оценить изменения во всех генах, которые рекомендуют проверять на мутации. Такое геномное профилирование опухоли помогает выбрать самый подходящий в конкретном случае вариант лечения8, 9. Современные методы лечения избирательно действуют на конкретные звенья процесса образования опухоли, благодаря этому можно точно «бить в цель» (таргетное воздействие, иммунотерапия), уничтожая только злокачественные клетки.
Какие ткани подходят для исследования методом КГП?
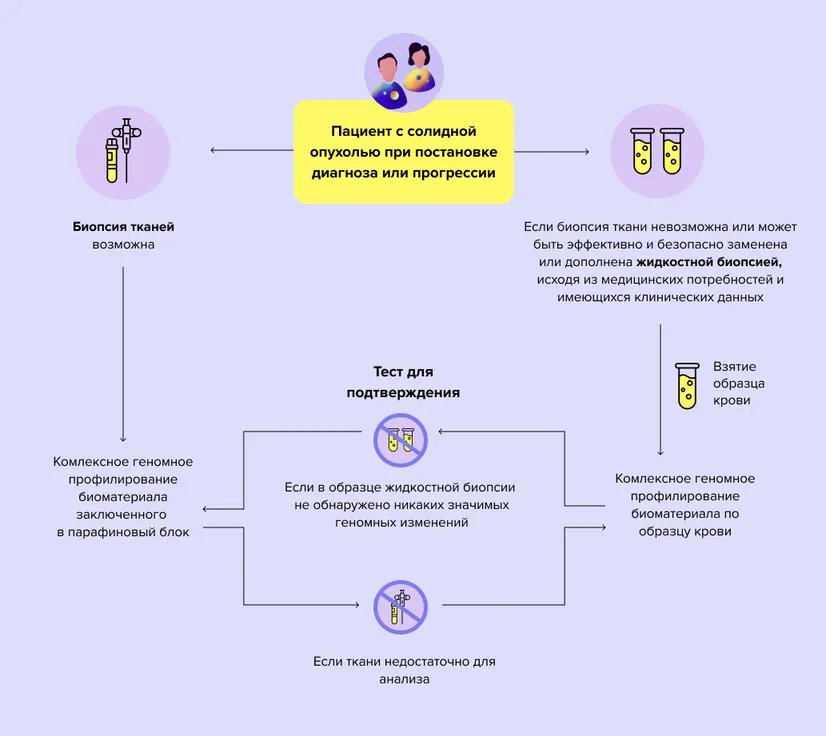
Для проведения тестирования подходят кусочки тканей опухоли, полученные при биопсии или во время операции. В случаях, когда биопсия ткани невозможна, или образца ткани недостаточно для анализа, можно использовать венозную кровь.
Кому показано проводить комплексное геномное профилирование?
В целом КГП показано для пациентов:
- с любым видом злокачественного новообразования III–IV стадии;
- и/или при опухолях, устойчивых к терапии;
- и/или при рецидивирующих опухолях;
- и/или при метастатических формах рака.
Особенно важно КГП для пациентов с опухолями невыявленной первичной локализации (ОНПЛ) и большой генетической разнородностью.
Как устроена система тестирования КГП
Комплексное геномное профилирование может состоять из нескольких этапов10, 11:
- Образцы исследуют на все клинически значимые генетические изменения с помощью секвенирования нового поколения NGS.
- Данные структурируют и получают практический результат с помощью биоинформационного анализа.
- Формируется подробный отчет с информацией о геномных изменениях в опухоли конкретного пациента и возможных персональных терапевтических подходах и вариантах таргетного лечения.
Каковы преимущества КПГ?
Инновационный метод геномного профилирования12:
- Комплексно оценивает все основные классы изменений в сотнях онкозначимых генов.
- Имеет высокую чувствительность и специфичность для ключевых геномных изменений.
- Комплексная панель подобрана на основании ведущих и проверенных в клинической практике научных рекомендаций, а также подтверждается биоинформатическим анализом.
- Итоговый подробный отчет дает четкое представление о геномном профиле опухоли пациента и позволяет подобрать ему персонализированное лечение.
- Быстрый ответ: от момента получения образца до отправки отчета врачу проходит менее двух недель.
Заключение
Современные научные достижения позволяют выявлять все типы молекулярных изменений в опухоли с высокой точностью. В результате врачи получают уникальный генетический профиль опухоли у каждого конкретного пациента. Благодаря этому они могут поставить точный диагноз, определить прогноз и выбрать оптимальное лечение, подходящее именно этому пациенту, то есть максимально индивидуализировать терапию. Комплексное геномное профилирование — инновационный подход, объединяющий в клинической практике новейшие методы диагностики, биоинформационный анализ и ведущих экспертов, чтобы каждый человек с онкологическим диагнозом мог получить лечение, которое подойдет именно ему и даст максимально эффективный результат.
Также читайте в нашей статье о видах мутаций и о том, при каких заболеваниях они могут встречаться.
M-RU-00009606 Март 2023
Было полезно?
Мы заботимся о том, чтобы наши материалы содержали актуальную информацию, а также оказывали читателям всю необходимую помощь и поддержку. Сообщите, пожалуйста, была ли эта статья полезна для вас.
Да, было полезно
Нет
Поделиться статьей
Список литературы
- Tsao A.S., Scagliotti G.V., Bunn Jr.P.A. J Thorac Oncol. 2016 May;11(5):613–638. DOI: 10.1016/j.jtho.2016.03.012.
- Global Oncology Trends Report 2018. Report by IQVIA Institute for Human Data Science. (Электронный ресурс.) https://www.iqvia.com/-/media/iqvia/pdfs/institute-reports/global-oncology-trends-2018.pdf (дата обращения: 11.10.2022).
- Murakami Y., et al. A screening method for the ALK fusion gene in NSCLC. Front. Oncol 2012. (Электронный ресурс.) https://doi.org/10.3389/fonc.2012.00024 (дата обращения: 04.06.2024).
- Illumina sequencing. (Электронный ресурс.) https://www.ebi.ac.uk/training/online/course/ebi-next-generation-sequencing-practical-course/what-next-generation-dna-sequencing/illumina- (дата обращения: 04.06.2024).
- Boussemart L., et al. Annals of Oncology. 2017;28(5):428–448.
- Ali S.M., et al. Oncologist. 2016;21:762–70.
- Schrock AB., et al. Clin Cancer Res. 2016;22:3281–5.
- Rotter J., Wilson L., Greiner M.A., et al. Shared-Patient Physician Networks and their Impact on the Uptake of Genomic Testing in Breast Cancer. Breast Cancer Res Treat. 2019 Jul;176(2):445–451. Published online 2019 Apr 26. DOI: 10.1007/s10549-019-05248-2.
- FoundationOne CDx Press Release. FDA companion diagnostic approval. (Электронный ресурс.) https://www.foundationmedicine.com/press-releases/f2b20698-10bd-4ac9-a5e5-c80c398a57b5 (дата обращения: 04.06.2024).
- Beaubier N., Bontrager M., Huether R., et al. Integrated genomic profiling expands clinical options for patients with cancer. Nature Biotechnology. 2019;37:1351–1360.
- Torres G.F., Bonilla C.E., Buitrago G., et al. How clinically useful is comprehensive genomic profiling for patients with non-small cell lung cancer? A systematic review. Crit Rev Oncol Hematol. 2021;166:103459. DOI: 10.1016/j.critrevonc.2021.103459.
- Woodhouse R., et al. Clinical and analytical validation of FoundationOne Liquid CDx, a novel 324-Gene cfDNA-based comprehensive genomic profiling assay for cancers of solid tumor origin. PLoS One. 2020;15(9):e0237802. DOI: 10.1371/journal.pone.0237802.
Под общим термином «рак» в действительности понимают огромное количество заболеваний. Более того, злокачественный процесс в одном органе может иметь множество подтипов. Например, один только подтип рака легкого, который называют немелкоклеточным, может запускать мутации как минимум в 13 изученных генах — они составляют основные 2/3 «виновников» этой болезни. А сколько генов, вовлеченных в развитие этой болезни, еще не изучено1?!
То есть существует множество молекулярных путей, сбой в которых приводит к тому, что нормальные клетки становятся злокачественными. Кроме того, в одной опухоли могут сочетаться разные мутации. С одной стороны, биологическое разнообразие опухолей — проблема, потому что нужно понять, какой вид заболевания у конкретного больного и из множества вариантов лечения выбрать оптимальный. С другой стороны, современные методы терапии позволяют прицельно воздействовать на конкретные молекулярные «поломки». И если точно подобрать «ключ», результат лечения будет очень хорошим.
Почему важно знать генетический профиль опухоли и связанные с ней мутации? Дело в том, что лечение рака очень усложнилось. В 2017 году в разработке находилось более 700 лекарственных молекул, действие которых направлено на разные пути образования опухолей2. Для подбора эффективного лекарства необходимо знать, какие именно генетические мутации есть в конкретном случае заболевания. Для этого проводят секвенирование — определение последовательностей «кирпичиков» (нуклеотидов), из которых состоит ДНК (генетический код) опухолевой клетки.
Секвенирование нового поколения расширяет возможности геномного профилирования опухолей
Передовой метод секвенирования нового поколения (с англ. NGS — next generation sequencing) дает возможность исследованием одного биоматериала провести комплексное геномное профилирование опухоли, т.е. обнаружить все возможные генетические изменения в большом количестве онкозначимых генов. При NGS происходит параллельное считывание миллионов мелких участков ДНК, их сравнение с эталонным геномом с помощью биоинформатического анализа.
Если с помощью прежних методов, таких как полимеразная цепная реакция (ПЦР), иммуногистохимическое исследование (ИГХ) или флуоресцентная гибридизация in situ (FISH) можно было исследовать изменения в одном или нескольких генах, то NGS позволяет исследовать практически весь геном за один раз3, 4.
Комплексное геномное профилирование — подход, объединяющий новейшие методы диагностики и лечения рака
С помощью КГП можно проанализировать все классы генетических изменений во всех известных онкозначимых генах. Таким образом, значительно повышается точность выявления мутаций в генах и определения типа опухоли. Так, КГП позволяет выявить до 37% больше пациентов с изменениями в генах при меланоме и до 35% больше при некоторых видах рака легкого по сравнению с методами ПЦР, ИГХ, FISH и другими традиционными методами5–7. Существуют тесты, позволяющие определить изменения (мутации) в 324 генах, связанных с раком.
КГП обеспечивает сопроводительную диагностику — дает информацию для безопасного и эффективного использования соответствующего лечения.
То есть, проведя один тест, можно оценить изменения во всех генах, которые рекомендуют проверять на мутации. Такое геномное профилирование опухоли помогает выбрать самый подходящий в конкретном случае вариант лечения8, 9. Современные методы лечения избирательно действуют на конкретные звенья процесса образования опухоли, благодаря этому можно точно «бить в цель» (таргетное воздействие, иммунотерапия), уничтожая только злокачественные клетки.
Какие ткани подходят для исследования методом КГП?
Для проведения тестирования подходят кусочки тканей опухоли, полученные при биопсии или во время операции. В случаях, когда биопсия ткани невозможна, или образца ткани недостаточно для анализа, можно использовать венозную кровь.
Кому показано проводить комплексное геномное профилирование?
В целом КГП показано для пациентов:
- с любым видом злокачественного новообразования III–IV стадии;
- и/или при опухолях, устойчивых к терапии;
- и/или при рецидивирующих опухолях;
- и/или при метастатических формах рака.
Особенно важно КГП для пациентов с опухолями невыявленной первичной локализации (ОНПЛ) и большой генетической разнородностью.
Как устроена система тестирования КГП
Комплексное геномное профилирование может состоять из нескольких этапов10, 11:
- Образцы исследуют на все клинически значимые генетические изменения с помощью секвенирования нового поколения NGS.
- Данные структурируют и получают практический результат с помощью биоинформационного анализа.
- Формируется подробный отчет с информацией о геномных изменениях в опухоли конкретного пациента и возможных персональных терапевтических подходах и вариантах таргетного лечения.
Каковы преимущества КПГ?
Инновационный метод геномного профилирования12:
- Комплексно оценивает все основные классы изменений в сотнях онкозначимых генов.
- Имеет высокую чувствительность и специфичность для ключевых геномных изменений.
- Комплексная панель подобрана на основании ведущих и проверенных в клинической практике научных рекомендаций, а также подтверждается биоинформатическим анализом.
- Итоговый подробный отчет дает четкое представление о геномном профиле опухоли пациента и позволяет подобрать ему персонализированное лечение.
- Быстрый ответ: от момента получения образца до отправки отчета врачу проходит менее двух недель.
Заключение
Современные научные достижения позволяют выявлять все типы молекулярных изменений в опухоли с высокой точностью. В результате врачи получают уникальный генетический профиль опухоли у каждого конкретного пациента. Благодаря этому они могут поставить точный диагноз, определить прогноз и выбрать оптимальное лечение, подходящее именно этому пациенту, то есть максимально индивидуализировать терапию. Комплексное геномное профилирование — инновационный подход, объединяющий в клинической практике новейшие методы диагностики, биоинформационный анализ и ведущих экспертов, чтобы каждый человек с онкологическим диагнозом мог получить лечение, которое подойдет именно ему и даст максимально эффективный результат.
Также читайте в нашей статье о видах мутаций и о том, при каких заболеваниях они могут встречаться.
M-RU-00009606 Март 2023
Было полезно?
Мы заботимся о том, чтобы наши материалы содержали актуальную информацию, а также оказывали читателям всю необходимую помощь и поддержку. Сообщите, пожалуйста, была ли эта статья полезна для вас.
Да, было полезно
Нет
Поделиться статьей
Список литературы
- Tsao A.S., Scagliotti G.V., Bunn Jr.P.A. J Thorac Oncol. 2016 May;11(5):613–638. DOI: 10.1016/j.jtho.2016.03.012.
- Global Oncology Trends Report 2018. Report by IQVIA Institute for Human Data Science. (Электронный ресурс.) https://www.iqvia.com/-/media/iqvia/pdfs/institute-reports/global-oncology-trends-2018.pdf (дата обращения: 11.10.2022).
- Murakami Y., et al. A screening method for the ALK fusion gene in NSCLC. Front. Oncol 2012. (Электронный ресурс.) https://doi.org/10.3389/fonc.2012.00024 (дата обращения: 04.06.2024).
- Illumina sequencing. (Электронный ресурс.) https://www.ebi.ac.uk/training/online/course/ebi-next-generation-sequencing-practical-course/what-next-generation-dna-sequencing/illumina- (дата обращения: 04.06.2024).
- Boussemart L., et al. Annals of Oncology. 2017;28(5):428–448.
- Ali S.M., et al. Oncologist. 2016;21:762–70.
- Schrock AB., et al. Clin Cancer Res. 2016;22:3281–5.
- Rotter J., Wilson L., Greiner M.A., et al. Shared-Patient Physician Networks and their Impact on the Uptake of Genomic Testing in Breast Cancer. Breast Cancer Res Treat. 2019 Jul;176(2):445–451. Published online 2019 Apr 26. DOI: 10.1007/s10549-019-05248-2.
- FoundationOne CDx Press Release. FDA companion diagnostic approval. (Электронный ресурс.) https://www.foundationmedicine.com/press-releases/f2b20698-10bd-4ac9-a5e5-c80c398a57b5 (дата обращения: 04.06.2024).
- Beaubier N., Bontrager M., Huether R., et al. Integrated genomic profiling expands clinical options for patients with cancer. Nature Biotechnology. 2019;37:1351–1360.
- Torres G.F., Bonilla C.E., Buitrago G., et al. How clinically useful is comprehensive genomic profiling for patients with non-small cell lung cancer? A systematic review. Crit Rev Oncol Hematol. 2021;166:103459. DOI: 10.1016/j.critrevonc.2021.103459.
- Woodhouse R., et al. Clinical and analytical validation of FoundationOne Liquid CDx, a novel 324-Gene cfDNA-based comprehensive genomic profiling assay for cancers of solid tumor origin. PLoS One. 2020;15(9):e0237802. DOI: 10.1371/journal.pone.0237802.
С помощью КГП можно проанализировать все классы генетических изменений во всех известных онкозначимых генах. Таким образом, значительно повышается точность выявления мутаций в генах и определения типа опухоли. Так, КГП позволяет выявить до 37% больше пациентов с изменениями в генах при меланоме и до 35% больше при некоторых видах рака легкого по сравнению с методами ПЦР, ИГХ, FISH и другими традиционными методами5–7. Существуют тесты, позволяющие определить изменения (мутации) в 324 генах, связанных с раком.
КГП обеспечивает сопроводительную диагностику — дает информацию для безопасного и эффективного использования соответствующего лечения.
То есть, проведя один тест, можно оценить изменения во всех генах, которые рекомендуют проверять на мутации. Такое геномное профилирование опухоли помогает выбрать самый подходящий в конкретном случае вариант лечения8, 9. Современные методы лечения избирательно действуют на конкретные звенья процесса образования опухоли, благодаря этому можно точно «бить в цель» (таргетное воздействие, иммунотерапия), уничтожая только злокачественные клетки.
Какие ткани подходят для исследования методом КГП?
Для проведения тестирования подходят кусочки тканей опухоли, полученные при биопсии или во время операции. В случаях, когда биопсия ткани невозможна, или образца ткани недостаточно для анализа, можно использовать венозную кровь.
Кому показано проводить комплексное геномное профилирование?
В целом КГП показано для пациентов:
- с любым видом злокачественного новообразования III–IV стадии;
- и/или при опухолях, устойчивых к терапии;
- и/или при рецидивирующих опухолях;
- и/или при метастатических формах рака.
Особенно важно КГП для пациентов с опухолями невыявленной первичной локализации (ОНПЛ) и большой генетической разнородностью.
Как устроена система тестирования КГП
Комплексное геномное профилирование может состоять из нескольких этапов10, 11:
- Образцы исследуют на все клинически значимые генетические изменения с помощью секвенирования нового поколения NGS.
- Данные структурируют и получают практический результат с помощью биоинформационного анализа.
- Формируется подробный отчет с информацией о геномных изменениях в опухоли конкретного пациента и возможных персональных терапевтических подходах и вариантах таргетного лечения.
Каковы преимущества КПГ?
Инновационный метод геномного профилирования12:
- Комплексно оценивает все основные классы изменений в сотнях онкозначимых генов.
- Имеет высокую чувствительность и специфичность для ключевых геномных изменений.
- Комплексная панель подобрана на основании ведущих и проверенных в клинической практике научных рекомендаций, а также подтверждается биоинформатическим анализом.
- Итоговый подробный отчет дает четкое представление о геномном профиле опухоли пациента и позволяет подобрать ему персонализированное лечение.
- Быстрый ответ: от момента получения образца до отправки отчета врачу проходит менее двух недель.
Современные научные достижения позволяют выявлять все типы молекулярных изменений в опухоли с высокой точностью. В результате врачи получают уникальный генетический профиль опухоли у каждого конкретного пациента. Благодаря этому они могут поставить точный диагноз, определить прогноз и выбрать оптимальное лечение, подходящее именно этому пациенту, то есть максимально индивидуализировать терапию. Комплексное геномное профилирование — инновационный подход, объединяющий в клинической практике новейшие методы диагностики, биоинформационный анализ и ведущих экспертов, чтобы каждый человек с онкологическим диагнозом мог получить лечение, которое подойдет именно ему и даст максимально эффективный результат.
Также читайте в нашей статье о видах мутаций и о том, при каких заболеваниях они могут встречаться.
M-RU-00009606 Март 2023
Было полезно?
Мы заботимся о том, чтобы наши материалы содержали актуальную информацию, а также оказывали читателям всю необходимую помощь и поддержку. Сообщите, пожалуйста, была ли эта статья полезна для вас.
Список литературы
- Tsao A.S., Scagliotti G.V., Bunn Jr.P.A. J Thorac Oncol. 2016 May;11(5):613–638. DOI: 10.1016/j.jtho.2016.03.012.
- Global Oncology Trends Report 2018. Report by IQVIA Institute for Human Data Science. (Электронный ресурс.) https://www.iqvia.com/-/media/iqvia/pdfs/institute-reports/global-oncology-trends-2018.pdf (дата обращения: 11.10.2022).
- Murakami Y., et al. A screening method for the ALK fusion gene in NSCLC. Front. Oncol 2012. (Электронный ресурс.) https://doi.org/10.3389/fonc.2012.00024 (дата обращения: 04.06.2024).
- Illumina sequencing. (Электронный ресурс.) https://www.ebi.ac.uk/training/online/course/ebi-next-generation-sequencing-practical-course/what-next-generation-dna-sequencing/illumina- (дата обращения: 04.06.2024).
- Boussemart L., et al. Annals of Oncology. 2017;28(5):428–448.
- Ali S.M., et al. Oncologist. 2016;21:762–70.
- Schrock AB., et al. Clin Cancer Res. 2016;22:3281–5.
- Rotter J., Wilson L., Greiner M.A., et al. Shared-Patient Physician Networks and their Impact on the Uptake of Genomic Testing in Breast Cancer. Breast Cancer Res Treat. 2019 Jul;176(2):445–451. Published online 2019 Apr 26. DOI: 10.1007/s10549-019-05248-2.
- FoundationOne CDx Press Release. FDA companion diagnostic approval. (Электронный ресурс.) https://www.foundationmedicine.com/press-releases/f2b20698-10bd-4ac9-a5e5-c80c398a57b5 (дата обращения: 04.06.2024).
- Beaubier N., Bontrager M., Huether R., et al. Integrated genomic profiling expands clinical options for patients with cancer. Nature Biotechnology. 2019;37:1351–1360.
- Torres G.F., Bonilla C.E., Buitrago G., et al. How clinically useful is comprehensive genomic profiling for patients with non-small cell lung cancer? A systematic review. Crit Rev Oncol Hematol. 2021;166:103459. DOI: 10.1016/j.critrevonc.2021.103459.
- Woodhouse R., et al. Clinical and analytical validation of FoundationOne Liquid CDx, a novel 324-Gene cfDNA-based comprehensive genomic profiling assay for cancers of solid tumor origin. PLoS One. 2020;15(9):e0237802. DOI: 10.1371/journal.pone.0237802.